Еще в 2021-08-24 гг. Cara Therapeutics и ее деловой партнер Vifor Pharma объявили, что ее первое вкладывающее агонист опиоидного рецептора каппа-опиоидных рецепторов (korsuva ™) был одобрен FDA для лечения хронической заболевания почек (КБД) (положительный модный/суровый покройте с гемодалисом, который ожидается, чтобы это было ожидается, что ожидается, что является ожидаемым 2022Q1. Cara и Vifor подписали эксклюзивное лицензионное соглашение для коммерциализации Korsuva ™ в Соединенных Штатах и согласились продать Korsuva ™ Fresenius Medical. Среди них Кара и Вифор имеют долю прибыли на 60% и 40% в доходе от продаж, кроме Fresenius Medical; Каждый имеет 50% доли прибыли в выручку от продаж от Fresenius Medical.
Ассоциированный ХБП зуд (CKD-AP) представляет собой генерализованный зуд, который происходит с высокой частотой и интенсивностью у пациентов с ХБП, перенесших диализ. Перерит встречается примерно у 60-70% пациентов, получающих диализ, из которых 30-40% имеют умеренный/тяжелый зуд, который серьезно влияет на качество жизни (например, плохое качество сна) и связано с депрессией. Ранее не было никакого эффективного лечения, связанного с ХБП, и одобрение дифференцированногофалина помогает устранить огромный разрыв в медицинской потребностях. Это одобрение основано на двух ключевых клинических испытаниях III фазы III в подаче NDA: положительные данные исследований Kalm-1 и Kalm-2 в США и во всем мире, а также поддерживающие данные из 32 дополнительных клинических исследований, которые демонстрируют, что Korsuva ™ хорошо переносится.
Не так давно Good News появилась из клинического исследования дификефалина в Японии: 2022-1-10, Cara объявила, что ее партнеры Maruishi Pharma и Kissey Pharma подтвердили, что инъекция дифференцированнойфалин используется в Японии для лечения зуда у пациентов с гемодиализом. Фаза III Клинические испытания Были выполнены первичная конечная точка. 178 пациентов получали 6 недель дифференцированногофалина или плацебо и участвовали в 52-недельном исследовании разгибания с открытым явлением. Первичная конечная точка (изменение в шкале численного рейтинга зуда) и вторичная конечная точка (изменение балла зуда по шкале тяжести ширатори) были значительно улучшены по сравнению с исходным уровнем в группе дифференцировки по сравнению с группой плацебо и были хорошо переносятся.
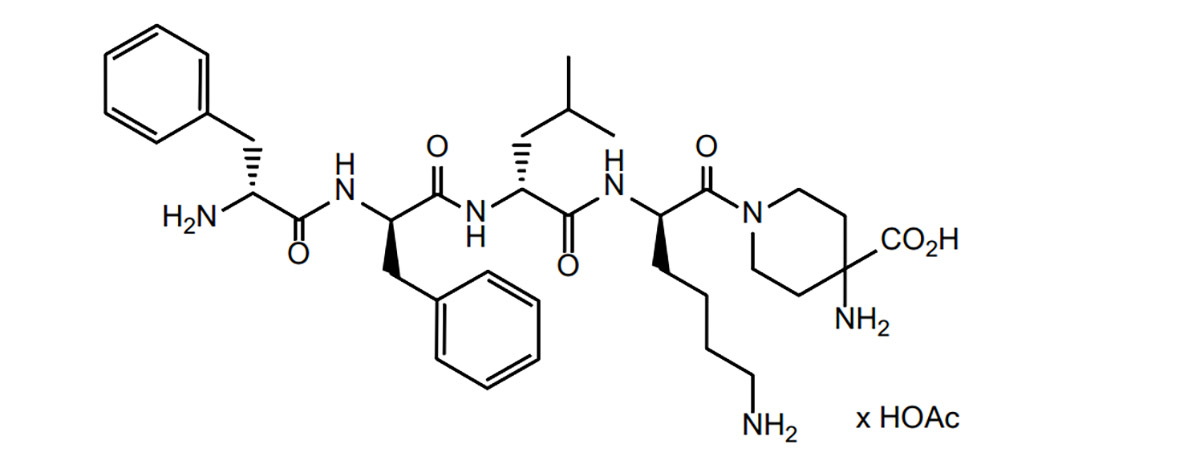
Difelikefalin - это класс опиоидных пептидов. Основываясь на этом, Peptide Research Institute изучил литературу по опиоидным пептидам и суммировал трудности и стратегии опиоидных пептидов в разработке лекарств, а также в текущей ситуации разработки лекарств.
Время публикации: 17-2022 февраля